Warum NICE wichtige Ergebnisse verschweigt
Brustkrebs ist die häufigste Form von Krebs bei Frauen. Deshalb ist es für sie besonders wichtig zu wissen, ob neuere Medikamente häufiger den Tod verhindern. Das englische NICE schwärzt in seiner Bewertung von Palbociclib aber ausgerechnet die Daten zum Überleben und findet das richtig so.
 Am 20.12.2017 veröffentlichte die englische „National Institute for Health and Care Excellence“ seine Bewertung von Palbociclib.1 Dabei sind die Daten zur Überlebenswahrscheinlichkeit nach ein, zwei und drei Jahren geschwärzt (siehe Abbildung). Till Bruckner von Transparimed2 wollte sich damit nicht abfinden und forderte kürzlich vom NICE nach dem britischen Freedom of Information Act die Herausgabe der Daten.3
Am 20.12.2017 veröffentlichte die englische „National Institute for Health and Care Excellence“ seine Bewertung von Palbociclib.1 Dabei sind die Daten zur Überlebenswahrscheinlichkeit nach ein, zwei und drei Jahren geschwärzt (siehe Abbildung). Till Bruckner von Transparimed2 wollte sich damit nicht abfinden und forderte kürzlich vom NICE nach dem britischen Freedom of Information Act die Herausgabe der Daten.3
Transparenz – nein Danke
Zwar räumte das NICE in seiner Antwort ein: „Zugunsten der Offenlegung erkennen wir an, dass es im öffentlichen Interesse ist, Transparenz und Verantwortlichkeit darüber herzustellen, wie NICE Technologiebewertungen durchführt und wie Pharmafirmen daran beteiligt sind.“4 Nur um fortzufahren: „Wir müssen jedoch berücksichtigen, dass die geschwärzte Information von Pfizer als kommerziell sensitiv betrachtet wird und dass die Offenlegung ihren Geschäftsinteressen schaden könnte.“
Aus dieser Antwort kann man eigentlich nur schließen, dass die geschwärzten Passagen für den Hersteller ungünstige Informationen zu dem Medikament enthalten. Wenn die vollmundigen Versprechen der Firma zum Nutzen von Palbociclib nicht zutreffen,5,6 könnte das in der Tat dem Umsatz schaden. Gleichwohl haben die von Brustkrebs betroffenen Frauen ein berechtigtes Interesse daran, vollständig über den tatsächlichen Nutzen und Schaden einer Behandlung informiert zu werden. Zumal die unerwünschten Wirkungen von Palbociclib erheblich sind.7
Immer schön brav
Damit nicht genug. Besonders krass ist die weitere Begründung von NICE. Da wird die Schwärzung damit begründet, dass ohne diese Vertraulichkeit die Unternehmen eventuell das Verfahren nicht mehr unterstützen würden und das könne nicht im öffentlichen Interesse sein.3 Zum Hintergrund: Im Gegensatz zum deutschen Nutzenbewertungsverfahren, dass die Hersteller per Gesetz dazu verpflichtet, die vollständigen Daten zu ihrem Präparat herauszurücken, geschieht das in England auf freiwilliger Basis. Das macht das NICE erpressbar – was zu beweisen war.
Der ganze Vorgang ist auch mit Blick auf die derzeitige Debatte über eine einheitliche europäische Nutzenbewertung wichtig, denn beim heutigen Stand des Gesetzentwurfs, sind weder die Verpflichtungen des Herstellers zur Lieferung der Daten von klinischen Studien noch die Transparenz des Bewertungsprozesses hinreichend klar geregelt. Der geschilderte Vorfall mag als Mahnung dienen, dass hier Rückschritte verhindert werden müssen. (JS)
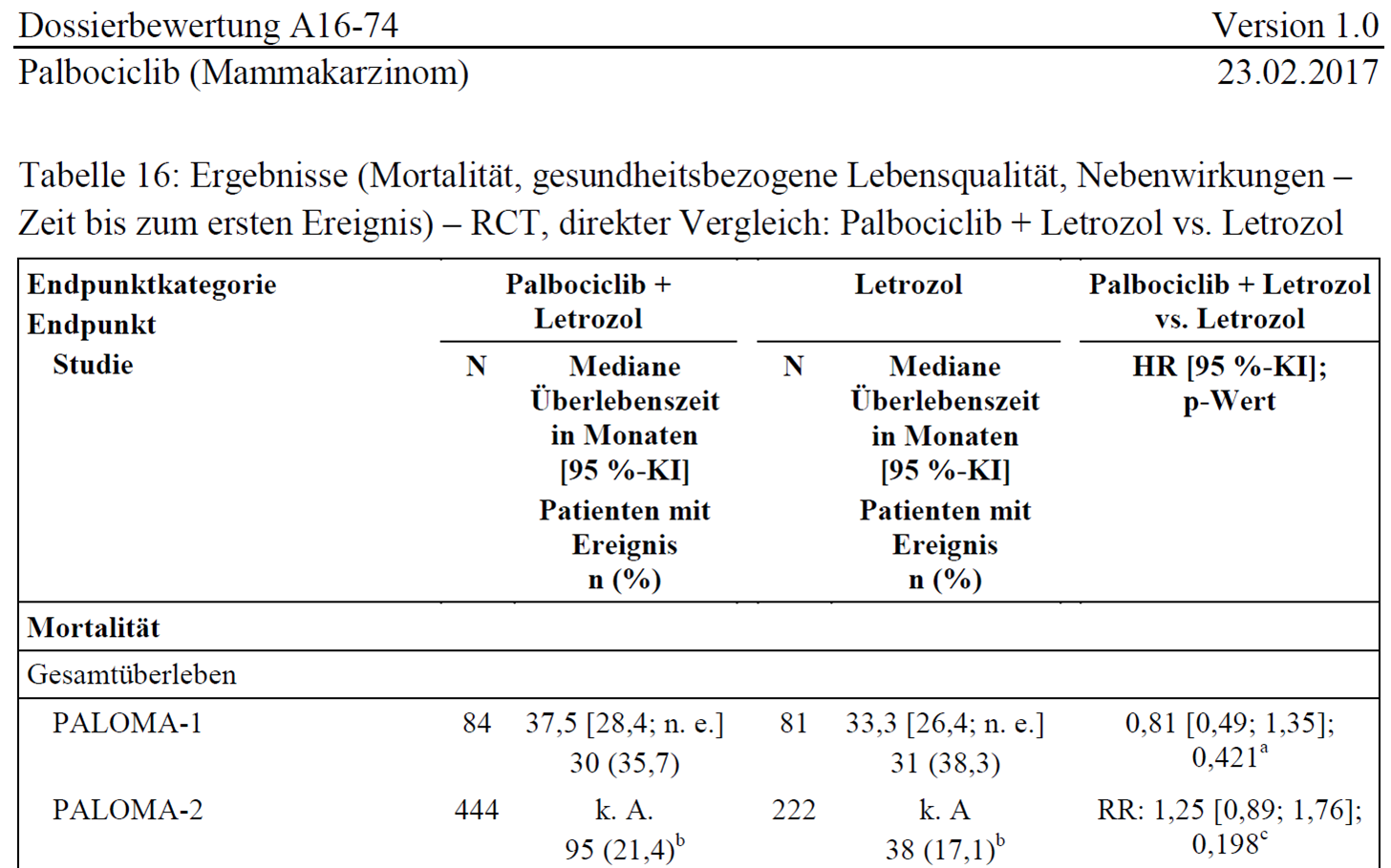 Zum Vergleich: Die Bewertung des deutschen "Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen"
Zum Vergleich: Die Bewertung des deutschen "Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen"

