Deutsche Unis hängen hinterher
Die Ergebnisse von klinischen Studien zu Arzneimitteln müssen 12 Monate nach Abschluss im europäischen Register EudraCT hinterlegt werden. Seit 2014 gilt diese Regel in der EU. Aber deutsche Unis haben nur bei 6,7% der fälligen Studien die Ergebnisse berichtet, in Großbritannien liegt die Quote dagegen bei 72,1%.[1] Das zeigt eine von TranspariMED und BUKO Pharma-Kampagne gemeinsam veröffentlichte Studie.[2]
Arzneimittelstudien an Menschen sind nicht ohne Risiken und deshalb streng reguliert. Ein klar benannter Sponsor trägt die Verantwortung für die korrekte Durchführung – und die anschließende Veröffentlichung. Hier geht es einmal nicht um die Pharmaindustrie, zumindest die großen Firmen kommen dieser Pflicht meist nach,[3] sondern um die deutschen Universitäten als Transparenzbremse.[4] In der europäischen Datenbank EudraCT[5] finden sich 477 klinische Studien deutscher Unis, die länger als 12 Monate abgeschlossen sind.[6] Aber nur von gerade einmal 32 Studien sind dort die Ergebnisse tatsächlich hinterlegt, 445 fehlen.[7] Es gibt allerdings große Unterschiede: während die Uni Münster deutlich über die Hälfte aller Resultate zugänglich gemacht hat, gibt es auch Unis von denen keinerlei Daten vorliegen (Ergebnisse im Detail siehe Kasten auf S. 3).
445 mal Ergebnis unbekannt
Klinische Studien sind ein Kernelement des medizinischen Fortschritts. Das gilt aber nur, wenn die Forschungsergebnisse auch lückenlos veröffentlicht werden. Ansonsten drohen falsche Behandlungsentscheidungen, weil Risiken oder Fortschritte unbekannt bleiben. Mit 68 unveröffentlichten Studienergebnissen ist die Berliner Charité Spitzenreiter bei der Intransparenz. Zum Beispiel wurde eine Studie zu grünem Teeextrakt bei Multipler Sklerose (MS) bereits im Februar 2016 abgeschlossen, die Resultate aber nicht in EudraCT eingestellt.[8] Auf Nachfrage teilte ein Mitglied des Forschungsteams mit, dass die statistische Auswertung gegenwärtig abgeschlossen würde und ein Eintrag in die Datenbanken und eine Publikation in Vorbereitung seien.[1] Bereits jetzt ist Eintrag in die EU-Datenbank um fast drei Jahre verzögert. Das ist unakzeptabel, da der Sinn des Registers ja gerade ist, dass wissenschaftliche Ergebnisse möglichst schnell bekannt werden. Die Publikation in Fachzeitschriften erfolgt häufig deutlich später als die für EudraCT gesetzte Frist von 12 Monaten.
Außerdem sind Artikel schon deshalb kein Ersatz 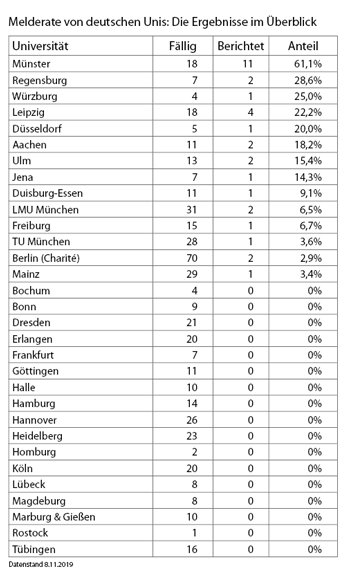 für den Eintrag ins Register, weil sie Ergebnisse selektiv und häufig verzerrt berichten. ForscherInnen der Universität Oxford überprüften 2015/16 die Veröffentlichungen zu Studien in fünf großen Fachzeitschriften . Nur 9 von 67 Studien wurden korrekt dargestellt. Insgesamt wurden die Ergebnisse zu 354 in der Studienplanung festgelegten Endpunkten nicht berichtet. Dagegen wurden 357 nachträgliche Auswertungen der Daten präsentiert, häufig ohne das kenntlich zu machen.[9]
für den Eintrag ins Register, weil sie Ergebnisse selektiv und häufig verzerrt berichten. ForscherInnen der Universität Oxford überprüften 2015/16 die Veröffentlichungen zu Studien in fünf großen Fachzeitschriften . Nur 9 von 67 Studien wurden korrekt dargestellt. Insgesamt wurden die Ergebnisse zu 354 in der Studienplanung festgelegten Endpunkten nicht berichtet. Dagegen wurden 357 nachträgliche Auswertungen der Daten präsentiert, häufig ohne das kenntlich zu machen.[9]
Die Universität Mainz untersuchte, ob die zusätzliche Gabe von Sunitinib die Prognose für PatientInnen mit Magenkrebs verbessert. Die Studie wurde sowohl in EudraCT[10] als auch im US-Register Clinicaltrials.gov registriert und endete im Juni 2013. Abgesehen davon, dass davon abgeraten wird, eine Studie in zwei Registern anzumelden, waren Ende 2018 in keinem von beiden die Ergebnisse hinterlegt. Immerhin gab es im August 2016 eine Zeitschriftenveröffentlichung: das Ergebnis der Studie war negativ.[11] Im US-Register ist immerhin erkennbar, dass der Sponsor versucht hatte, im August 2018 die Daten hochzuladen. Wegen Inkonsistenzen hatte Clinicaltrials.gov am 24.1.2019 an den Sponsor Nachfragen geschickt, die offensichtlich bis heute nicht beantwortet wurden.[12] Offensichtlich hat unser Bericht etwas bewegt: Im Januar 2020 hat die Uni Mainz die Studienergebnisse im europäischen Register eingestellt.
Die Universität Hannover erforschte, ob Botulinumtoxin gegen Depressionen hilft. Die Studie wurde im Dezember 2011 beendet. Bis heute wurde das Ergebnis weder in EudraCT hinterlegt,[13] noch gibt es eine Veröffentlichung zu den Resultaten in einer medizinischen Fachzeitschrift.1 Angesichts der unklaren Evidenzlage, ob Botulinumtoxin eine Therapieoption bei Depressionen sein kann, ist die fehlende Veröffentlichung besonders bedauerlich.
Flaue Ausreden
Bei einer weiteren Charité-Studie zu MS mit dem Wirkstoff Fingolimod, deren Ergebnisse spätestens im August 2019 in EudraCT hätten stehen müssen,[14] rechtfertigten sich die ForscherInnen damit, dass vorläufige Ergebnisse bei Kongressen vorgestellt worden sein. Das ist zwar ein erster Schritt, ersetzt aber keinesfalls die rechtzeitige Veröffentlichung im EU-Register.
Einige Universitäten, aber auch das für die Arzneimittelzulassung mit zuständige Paul Ehrlich Institut (PEI) vertraten die Auffassung, dass die Veröffentlichung der Studienergebnisse gar nicht rechtlich vorgeschrieben sei. Denn die seit 2014 gültige Vorschrift der Einstellung in das EU-Portal 12 Monate nach Abschluss der Studie sei nur in einer EU-Leitlinie von 2012 verankert.[15]
Die deutsche Zulassungsbehörde BfArM teilt dagegen die Auffassung der EU-Kommission, der Konferenz der europäischen Behörden und der EMA, dass diese Leitlinie rechtlich bindend ist. Denn sie regelt die praktische Umsetzung von zwei EU-Verordnungen von 2002 und 2004. Beide hatten eine Veröffentlichungspflicht bereits im Grundsatz festgeschrieben.[16] EU-Verordnungen aber haben unmittelbare Rechtskraft in allen Mitgliedsstaaten.
Müßige Debatte
Abgesehen davon, dass es im Sinne des PatientInnenwohls nicht zu rechtfertigen ist, Studienergebnisse zu verschweigen, lässt die EU-Verordnung zu klinischen Studien von 2014 künftig gar keinen Spielraum mehr.[17] Sie schreibt die Pflicht zur Veröffentlichung der Zusammenerfassung der Ergebnisse vor. Darüber hinaus gilt für alle Studien, die bei einem Zulassungsverfahren eingereicht wurden, dass die Clinical Study Reports, die die vollständigen Ergebnisse einer Studie enthalten, einen Monat nach dem Abschluss (oder der Einstellung) des Verfahrens in eine öffentliche EU-Datenbank eingestellt werden muss.
Dass diese neuen weitergehenden Regelungen noch nicht gültig sind, hat mit einer Kuriosität in der Verordnung zu tun. Eigentlich sollte sie frühestens am 28. Mai 2016 in Kraft treten, allerdings nicht bevor das EU-Datenportal voll funktionsfähig ist.[18] Das sollte nach den Planungen der EMA ursprünglich Dezember 2017 fertig sein, jetzt sieht es eher danach aus, dass das erst Ende 2020 der Fall sein wird,[19] – ein Armutszeugnis für die EMA und die EU-Kommission.
Forschungsmüll
Wenn die Ergebnisse öffentlich geförderter Forschung nicht zeitgerecht oder gar nicht veröffentlicht werden, ist das nicht nur eine Verschwendung von Steuergeldern, es schadet auch PatientInnen, da Gefahren oder fehlende Wirksamkeit nicht bekannt werden. Außerdem kann die Nichtveröffentlichung zur unnötigen Wiederholung von Studien mit den gleichen Wirkstoffen führen. Prof. Jürgen Windeler, Chef des Instituts für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) fordert deswegen, den Berichtsverweigerern die öffentliche Förderung zu sperren.
Untersuchung zeigt Wirkung
Zum Glück scheint bei einigen Universitäten die Botschaft angekommen zu sein. Nicht zuletzt aufgrund der Nachfragen von TranspariMED und der Presse im Rahmen der hier vorgestellten Untersuchung sind einige Unis aktiv geworden. Während die Uni Hannover zum Stichpunkt für die Datenerhebung Anfang November 2019 keine einzige der 26 fälligen Studien eingestellt hatte, waren einen Monat später bereits für 5 Studien die Ergebnisse hochgeladen. Gegenüber der Süddeutschen Zeitung „verwiesen die Charité und die Kliniken der Universitäten in München und Freiburg darauf, dass sie derzeit Strukturen etablieren, die sich der besseren Koordination klinischer Studien und ihrer Veröffentlichung widmen.“ [20]
Aufgrund der Kritik von TranspariMED und der Pharma-Kampagne hat das PEI jetzt immerhin deutlich gemacht, dass es die zeitgerechte Veröffentlichung von Studienergebnissen für eine wichtige Sache hält. „Das Paul-Ehrlich-Institut (PEI), Bundesinstitut für Impfstoffe und biomedizinische Arzneimittel, unterstützt diese Forderung ausdrücklich“, ließ das Institut am 2.1.2020 die Öffentlichkeit wissen.[21]
Dr. Susanne Johna, 1. Vorsitzende des Marburger Bundes, dem größten deutschen ÄrztInnenverband, reagierte ebenfalls auf unsere Untersuchung: „Die Ergebnisse klinischer Forschung müssen öffentlich zugänglich sein. Es ist völlig inakzeptabel, wenn Universitäten dieser Verpflichtung zur Transparenz nur unzureichend nachkommen. […] Die betroffenen Universitäten müssen sich fragen lassen, ob sie insbesondere negative Studienergebnisse zurückhalten. Mit ihrem Verhalten schaden sie auch sich selbst. Die Universitäten enttäuschen Patienten und Probanden, die für klinische Studien auch mit dem Argument gewonnen werden, dass sie zur Weiterentwicklung von Therapien beitragen können.“[22] (JS)
Artikel aus dem Pharma-Brief 1/2020, S.1
Screenshot: https://www.bukopharma.de/images/aktuelles/CT_Transparency_German_Uni_2019.pdf
[1] Die genannten Prozentzahlen beziehen sich auf die tatsächlich gemeldeten Ergebnisse, diese sind in nicht wenigen Fällen aber nicht zeitgerecht, also nach 12 Monaten berichtet worden.
[2] TranspariMed und BUKO Pharma-Kampagne (2019) Clinical trials transparency at German universities. Bielefeld and Bristol. 30. Nov. www.bukopharma.de/images/aktuelles/CT_Transparency_German_Uni_2019.pdf
[3] Bei mittleren und kleinen Firmen sieht es europaweit auch eher schlecht aus. Fehlende Ergebnisse in EudraCT: Mittlere Firmen 23%, kleine Firmen 66%. Bruckner T (2019) Most clinical trials run by small companies are missing results. TranspariMED. 1 Nov. www.transparimed.org/single-post/2019/11/01/Most-clinical-trials-run-by-small-companies-are-missing-results [Zugriff 14.1.2020]
[4] Nach Angaben der EU lag im April 2019 die Berichtsquote bei kommerziellen Sponsoren bei 77,2% gegenüber 23,6% bei nicht-kommerziellen Sponsoren. www.bfarm.de/DE/Arzneimittel/Arzneimittelzulassung/KlinischePruefung/news/Ergebnisberichte.html [Zugriff 9.1.2020]
[5] www.clinicaltrialsregister.eu/ctr-search/search
[6] Besser durchsuchbar und auswertbar sind die Daten von EudraCT im EU Trials Tracker der Uni Oxford: http://eu.trialstracker.net/
[7] Stand 8. November 2019. Details zur Datenerfassung siehe Fußnote 1
[8] www.clinicaltrialsregister.eu/ctr-search/trial/2008-005213-22/DE [Zugriff 7.1.2020]
[9] https://compare-trials.org/ [Zugriff 14.1.2020]
[10] www.clinicaltrialsregister.eu/ctr-search/search?query=2009-014336-38 [Zugriff 27.1.2020]
[11] Moehler et al. (2016) BMC Cancer; 16, 699 https://bmccancer.biomedcentral.com/articles/10.1186/s12885-016-2736-9
[12] https://clinicaltrials.gov/ct2/show/results/NCT01020630 [Zugriff 27.1.2020]
[13] www.clinicaltrialsregister.eu/ctr-search/search?query=2009-015125-36 [Zugriff 27.1.2020]
[14] www.clinicaltrialsregister.eu/ctr-search/search?query=2012-000411-91 [Zugriff 27.1.2020]
[15] Leitlinie 2012/302 03/EG
[16] Umsetzung von Artikel 57 Absatz 2 der Verordnung (EG) Nr. 726/2004 und Artikel 41 Absatz 2 der Verordnung (EG) Nr. 1901/2006
[17] Verordnung (EG) Nr. 536/2014
[18] Die EU-Verordnung tritt in Kraft sechs Monate nachdem die Funktionsfähigkeit des EU-Portals bestätigt und im Amtsblatt der EU veröffentlicht ist.
[19] EMA (2019) EMA Management Board: highlights of December 2019 meeting www.ema.europa.eu/en/news/ema-management-board-highlights-december-2019-meeting [Zugriff 27.1.2020]
[20] Bernd C und Grill M (2019) In Deutschland erforscht, im Nirwana versunken. Süddeutsche Zeitung 29. Dez. www.sueddeutsche.de/gesundheit/veroeffentlichung-studien-1.4737316
[21] PEI (2020) Gemeinsames Schreiben der Europäischen Kommission, der EMA und der HMA an die Verantwortlichen von klinischen Prüfungen zu den Erfordernissen, die Ergebnisse ihrer genehmigten klinischen Studien in EudraCT bereitzustellen (Juni 2019). Positionen 2. Jan. www.pei.de/DE/newsroom/positionen/200102-veroeffentlichung-ergebnisse-klinischer-studien.html [Zugriff 9.1.2020]
[22] Marburger Bund (2020) Ergebnisse klinischer Studien müssen transparent sein. Pressemitteilung 3. Jan. www.marburger-bund.de/bundesverband/pressemitteilung/ergebnisse-klinischer-studien-muessen-transparent-sein [Zugriff 10.1.2020]

