IQWiG zieht Bilanz nach 7 Jahren Bewertung
Das Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) kommt zu einem ernüchternden Urteil: Nur wenige neue Arzneimittel bringen PatientInnen substanzielle Vorteile. Das Institut bleibt aber nicht bei einer Analyse stehen, es fordert eine Umorientierung der Medikamentenforschung.[1]
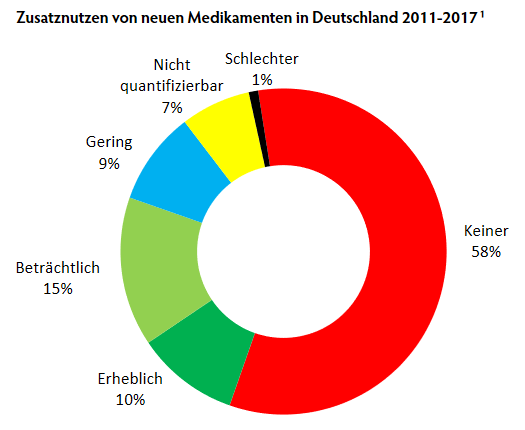
Seit 2011 müssen alle neuen Medikamente, die in Deutschland auf den Markt kommen, auf ihren Zusatznutzen bewertet werden. Für die wissenschaftliche Bewertung ist mit wenigen Ausnahmen[2] das IQWiG zuständig, die endgültigen Entscheidungen trifft der Gemeinsame Bundesausschuss (G-BA).[3] Von 2011 bis 2017 wurden 216 Medikamente durch das Institut bewertet, davon waren 152 neue Wirkstoffe und 64 neue Indikationen. Für 125 der Medikamente (58%) wurden keine Daten vorgelegt, die eine Verringerung der Sterblichkeit, der Symptome oder Verbesserung der Lebensqualität bestätigt hätten. Zwei Mittel (1%) waren sogar schlechter als die etablierte Vergleichstherapie.
Nur einem Viertel der Neueinführungen (54 Mittel) konnte ein beträchtlicher oder erheblicher Zusatznutzen bescheinigt werden. 16% (35) hatten einen geringen oder nicht quantifizierbaren Zusatznutzen. Ein genauerer Blick relativiert selbst diese Zahlen. Denn bei knapp der Hälfte (42%) dieser Mittel konnte eine Verbesserung nur für bestimmte PatientInnengruppen festgestellt werden.
Am schlechtesten schneiden Psychopharmaka (nur 6% mit Zusatznutzen) und Mittel gegen Diabetes ab (17% mit Zusatznutzen). Auffällig ist das Ungleichgewicht bei den Anwendungsgebieten: über ein Drittel (82) sind Krebsmedikamente. Diese schneiden bei der Bewertung deutlich besser ab, 59% konnte ein Zusatznutzen bescheinigt werden. Ähnliches gilt für die zweitgrößte therapeutische Gruppe, den 29 Mitteln gegen Infektionen (vor allem Hepatitis C und HIV), 62% mit Zusatznutzen.
Ungewissheit
Was verbirgt sich hinter der großen Gruppe von Medikamenten, denen kein Zusatznutzen bescheinigt werden konnte? In vielen Fällen sorgen ungeeignete Studien für ein negatives Urteil. Wenn nur gegen Placebo getestet wurde (64 Mittel), statt gegen eine Vergleichstherapie, kann man gar nicht beurteilen, ob das Medikament schlechter, besser oder gleichgut wirkt. Ebenfalls häufig (42 Mittel) war in den Studien ein ungeeignetes Vergleichsmedikament gewählt worden (für die Indikation gar nicht zugelassen, ungeeignete Dosis gewählt u.a.). 19 Medikamente waren nicht besser als die etablierte Therapie.
Auch die Hoffnung, dass nach Zulassung weiter geforscht wird und sich die die Ungewissheit dadurch auflöst, erfüllt sich selten. Entweder werden geeignete Studien gar nicht erst durchgeführt oder die Endergebnisse[4] bzw. besser gemachte Studien zeigen dann keinen zusätzlichen Nutzen.
Auf jeden Fall macht die Ungewissheit über den Nutzen bei Zulassung vernünftige Therapieentscheidungen schwierig.
Mehr vom Gleichen
Auffällig ist die große Ähnlichkeit etlicher erfolgreicher neuer Medikamente, die auf dem gleichen Wirkprinzip basieren. So sind ein Viertel aller positiv bewerteten Krebsmedikamente PD-1 oder PD-L1 Inhibitoren, weitere befinden sich in der Forschungspipeline. Alle neuen Hepatitis C-Medikamente basieren auf direkter antiviraler Wirkung. Das stellt eine Verschwendung von Forschungsgeldern dar (die die Allgemeinheit über hohe Medikamentenpreise refinanziert).
Neue Lösungen gefragt
Die drei MitarbeiterInnen des IQWiG formulieren klare Änderungsvorschläge. Als erster Schritt wird ein Umdenken bei der Zulassung gefordert. Es sollten wieder ausreichend große Phase III-Studien durchgeführt werden, die Ergebnisse messen, die für PatientInnen relevant sind (und nicht nur die Verbesserung von Laborwerten). Um Daten für eine Nutzenbewertung zu gewinnen, sollte – wo möglich – gegen die etablierte Therapie verglichen werden. Bei Entscheidungen über die Erstattung und Preise dürften marginale Fortschritte und unsichere Ergebnisse nicht belohnt werden.
Langfristig müsse die Gesundheitspolitik eine aktivere Rolle übernehmen: Statt passiv darauf zu warten, was die Pharmaindustrie entwickelt, sollte die Gesellschaft selbst Prioritäten für die Forschung setzen. Ein Vergleich mit der Entwicklungspipeline der Industrie mit dem tatsächlichen Bedarf kann Lücken identifizieren. Öffentlich finanzierte Forschungsprogramme können eine wirksame Maßnahme sein. Das beweist für die vernachlässigten Krankheiten bereits seit einiger Zeit die Drugs for Neglected Diseases initiative (DNDi), die erfolgreich Medikamente für Tropenkrankheiten entwickelt. Im Bereich der Antibiotikaforschung sind die WHO und auch die Bundesregierung aktiv geworden. Auch andere Modelle wie Forschung als öffentliches Unternehmen oder Open Source böten vielversprechende Möglichkeiten. (JS)
Artikel aus dem Pharma-Brief 4-5/2019, S.13
[1] Wieseler B et al. (2019) New drugs: where did we go wrong and what can we do better? BMJ; 366, p i4340
[2] Medikamente gegen seltene Krankheiten (Orphan Drugs) werden bis zu einem Jahresumsatz von 50 Mio. € durch den G-BA selbst bewertet. Dabei gilt aufgrund der gesetzlichen Vorgaben (AMNOG) ein fiktiver Zusatznutzen als belegt. Der G-BA kann nur noch das Ausmaß festlegen bzw. entscheiden, dass er einen Zusatznutzen nur aus rein rechtlichen Verpflichtungen erteilt.
[3] Pharma-Brief (2013) Ein Erfolgsmodell soll abgeschafft werden. Nr. 8-9, S. 6
[4] Pharma-Brief (2019) Die nächste Schlappe. Nr. 2, S. 6